Foto: Divulgação
A Zenas BioPharma, uma empresa biofarmacêutica global comprometida em se tornar líder no desenvolvimento e comercialização de terapias imunológicas para pacientes necessitados em todo o mundo, anunciou neste domingo (15) que solicitou a aprovação de um novo investigacional (IND) à Administração Nacional de Produtos Médicos da China (NMPA) para o início de um estudo clínico de Fase 1/2 do ZB001 para o tratamento da Doença Ocular da Tireoide (TED). Este estudo foi projetado para avaliar a segurança, tolerabilidade, farmacocinética e eficácia preliminar do ZB001.
‘A solicitação de aprovação do ZB001 IND ao NMPA é um marco significativo para a Zenas’, disse Hua Mu, MD, PhD, Diretor Executivo da Zenas. ‘No momento não existe nenhuma terapia aprovada para pacientes com TED na China. As opções de tratamento são limitadas e muitas vezes envolvem altas doses de esteroides que resultam em efeitos colaterais graves ou intervenção cirúrgica. O ZB001 tem o potencial de mudar o paradigma do tratamento para pacientes com TED na China.’
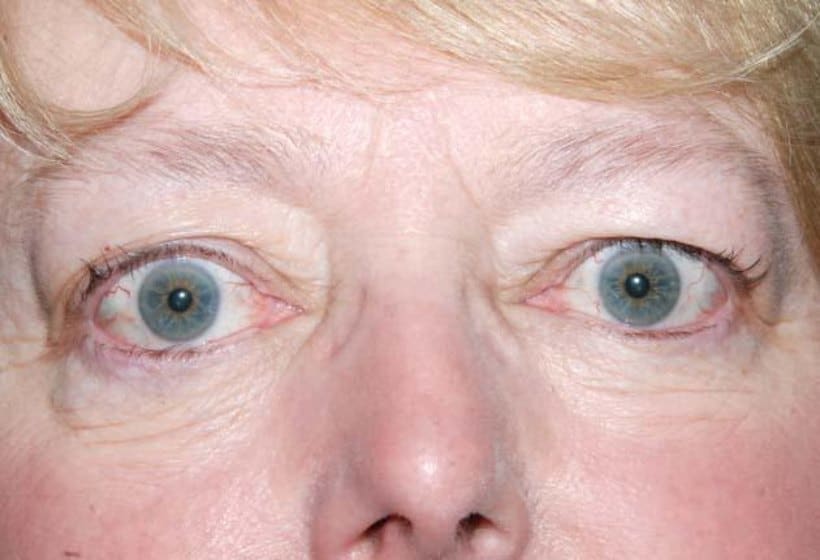
O ZB001 é um anticorpo monoclonal humanizado diferenciado que direciona o receptor de fator de crescimento semelhanteàinsulina 1 (IGF-1R) para o tratamento de TED. TED é uma doença autoimune debilitante que causa inflamação e fibrose dentro da órbita do olho, podendo causar visão dupla, dor e cegueira em potencial. Pacientes com doença grave muitas vezes requerem múltiplas cirurgias corretivas da órbita, músculos dos olhos e pálpebras.
A Zenas BioPharma licenciou os direitos exclusivos para desenvolver, fabricar e comercializar o ZB001 e outros compostos direcionados ao IGF-1R em indicações não oncológicas na Grande China da Viridian Therapeutics, Inc. (Viridian) em outubro de 2020. Em novembro de 2021, a Viridian solicitou um IND para o ZB001 (VRDN-001 na Viridian)àFood and Drug Administration dos EUA e, em dezembro de 2021, deu início a um ensaio clínico de Fase 1/2 para avaliar a prova de conceito em pacientes com TED nos EUA.
Sobre a Zenas BioPharma
A Zenas BioPharma é uma empresa biofarmacêutica mundial com sedes nos EUA e na China, comprometida em se tornar líder global no desenvolvimento e comercialização de terapias imunológicas para pacientes nos EUA, China e em todo o mundo. A Zenas está avançando rapidamente um vasto pipeline de terapêuticas inovadoras que continua a crescer por meio da nossa estratégia de desenvolvimento de negócios de sucesso. Nossa experiente equipe de liderança e rede de parceiros de negócios impulsionam a excelência operacional para oferecer terapias potencialmente transformadoras para melhorar a vida das pessoas que enfrentam doenças autoimunes e raras.
Para mais informação sobre a Zenas BioPharma, visite www.zenasbio.com siga no Twitter em e LinkedIn.
Com informações da Agência Estado
Não deixe de curtir nossa página no Facebook, siga no Instagram e também no X.






